EMA permite uso de tratamiento Covid-19 de Pfizer
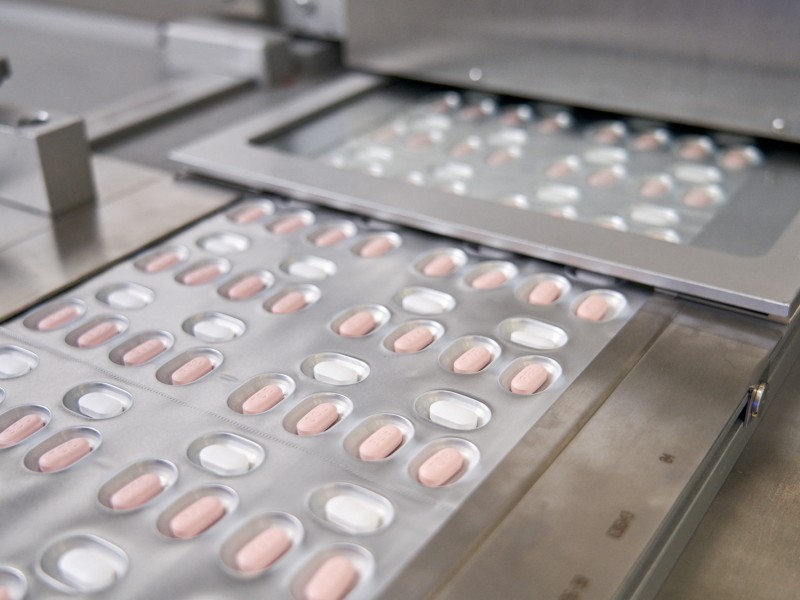
Ante la nueva ola Covid-19 que afecta a todo el continente europeo, la EMA permitió que todos los estados miembros utilicen el tratamiento anti Covid-19 "Paxlovid" de la farmacéutica Pfizer.

Este jueves, a través de un comunicado, la Agencia Europea de Medicamentos (EMA) informó que permitió que los estados miembros de la Unión Europea utilizan la pastilla anti Covid-19 de Pfizer, esto mucho antes de su aprobación formal, una medida de emergencia necesaria ante la presencia de una nueva ola de contagios en todo ese continente.
Esta determinación por parte de la EMA, llega luego de que Pfizer anunciara que los resultados preliminares de un ensayo clínico de su tratamiento "Paxlovid" redujera las hospitalizaciones y muertes de personas de riesgo hasta en un 90% frente a la variante Ómicron.
"El fármaco, que aún no está autorizado en la UE, puede utilizarse para tratar a los adultos con COVID-19 que no requieren oxígeno suplementario y que tienen un mayor riesgo de desarrollar una forma grave de la enfermedad", dijo la EMA en un comunicado.
Bajo la hipótesis de que la presencia de la variante Ómicron y la permanencia de otras mutaciones como la Delta fueran las causantes de su nueva ola de contagios, la agencia explicó que emitió la recomendación para apoyar a las autoridades nacionales y prevenir el desbordamiento hospitalario o inclusive un alza en los índices de muerte.
ESPECIFICACIONES TÉCNICAS
El Paxlovid, es una combinación de una nueva molécula, el compuesto PF-07321332 y el antirretroviral ritonavir, que se utiliza contra el virus del SIDA. "Paxlovid debería ser administrada lo antes posible tras el diagnóstico del COVID-19 en los cinco primeros días desde el inicio de los síntomas", indicó la EMA que agregó que el tratamiento debe extenderse durante cinco días más.
EFECTOS SECUNDARIOS
Los efectos secundarios más comunes son perturbaciones en el gusto, diarrea y vómitos.
CONTRAINDICACIONES
Este compuesto no debe ser administrado a mujeres embarazadas y la lactancia debe ser interrumpida, en caso de su utilización.
EL DATO...
El pasado 13 de diciembre, la EMA lanzó un examen acelerado de una autorización de comercialización.
La agencia sanitaria europea ya emitió una aprobación de emergencia similar para el tratamiento desarrollado por Merck.

