Replica Coepriss alerta sanitaria sobre la falsificación del medicamento Roactemra
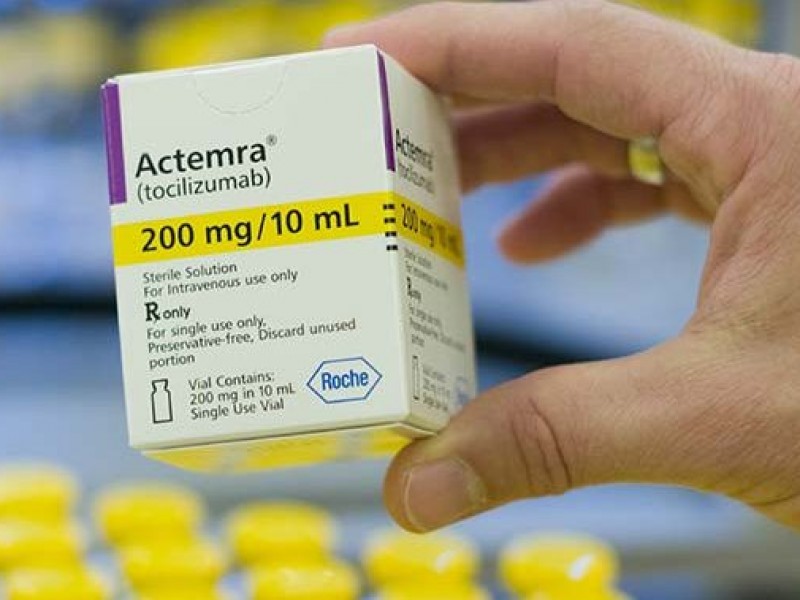
El comisionado estatal para la Protección contra Riesgos Sanitarios de Sinaloa (Coepriss), Jorge Alan Urbina Vidales, replicó la información emitida a nivel federal por la Secretaría de Salud, a través de Cofepris, sobre la falsificación del medicamento Roactemra (Tocilizumab).
El titular de Coepriss informó que la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) ha realizado una investigación a partir de información proporcionada por Instituciones de Salud y las denuncias interpuestas por la empresa Productos Roche, S.A. de C.V., para el producto RoActemra (Tocilizumab) solución 80mg/4mL inyectable M.B., caja con 1 frasco ámpula de 4mL, y RoActemra (Tocilizumab) solución 200mg/10mL, caja con 1 frasco ámpula de 10mL.
"Se recomienda a la población en general que antes de adquirir el producto inspeccione el etiquetado del mismo, su contenido y, en caso de identificar alguno de los lotes reportados, se recomienda no adquirirlo. Si tiene en uso, deberá revisarlo y constatar que sea original; de tener sospecha, deberá suspender la aplicación", advirtió.
Precisó que la empresa Productos Roche, S.A. de C.V., realizó el análisis comparativo de estos productos, concluyendo que los productos recuperados son falsificados.
Cabe señalar que el producto RoActemra (Tocilizumab) identificado por la empresa Productos Roche, S.A. de C.V., como falsificado ostenta la siguiente información:
Lotes B2080B04 con fecha de caducidad 09 AGO 2020, y B2096B03 con fecha de caducidad 17 ABR 2021, de la presentación solución 80mg/4mL inyectable MB, caja con 1 frasco ámpula de 4mL.
Lote B2078B01 con fecha de caducidad 24 OCT 2020, de la presentación solución 200mg/10mL, caja con 1 frasco ámpula de 10mL.
Jorge Alan Urbina Vidales apuntó que el medicamento original RoActemra, según información proorcionada por Roche, está indicado para el tratamiento de la artritis reumatoide (AR) activa de intensidad moderada a grave, en pacientes adultos, y en el tratamiento de la artritis Idiopática juvenil sistémica en pacientes a partir de los 2 años de edad y es un producto con registro sanitario 044M2009 SSA IV.
Sostuvo que como parte del proceso interno y del análisis efectuados por la empresa Productos Roche, S.A. de C.V., se señalan las diferencias encontradas en las piezas recuperadas de los siguientes lotes del producto RoActemra (Tocilizumab) falsificado:
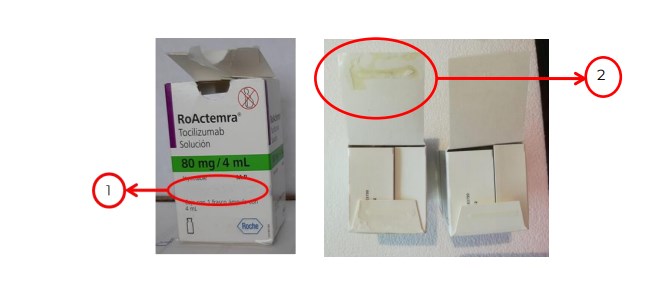
En el empaque secundario (caja de cartón): 1. Carece de dos leyendas impresas 2. Pegamento adicional en la solapa inferior del empaque secundario. No presentan los insertos correspondientes (instructivo para el usuario e instructivo para el profesional de salud)
En el empaque primario (vial): 1. El tamaño del tapón de plástico del vial es mayor con respecto al original 2. Visibles daños en el casquillo y en la tapa del vial muestra señales de maltrato a nivel de los sujetadores 3. Las piezas recuperadas no cuentan con etiqueta de identificación, los viales resultaron de color ámbar o transparente, tienen o no, tapa flip-off de color diferente (p.ej. amarillo o rojo), tamaño y forma desigual respecto al original, difieren en el color del casquillo
Finalmente, en lo que se refiere al prroducto: 1. El volumen del líquido contenido en el vial, puede ser menor o mayor con respecto al original, líquido incoloro con presencia de sólido con apariencia de crecimiento microbiano o líquido colorido.
Jorge Alan Urbina Vidales subrayó que de encontrar alguna de estas diferencias o ante cualquier sospecha de falsificación el producto no debe ser usado y debe procederse a realizar la denuncia sanitaria en la siguiente página de internet: https://www.gob.mx/cofepris/acciones-y-programas/denuncias-sanitarias, para ello es importante tener a la mano el recibo de compra del producto.
"Las farmacias y puntos de venta saben que deben adquirir el medicamento a través de distribuidores autorizados, y en este caso se les pide verificar que la información y documentación del medicamento no esté relacionada con estos lotes", enfatizó.
El comisionado subrayó que debe reportarse cualquier reacción adversa o malestar asociado al uso o consumo de este producto en la liga electrónica "¿Te hizo daño un medicamento?" de la página web de la Cofepris https://www.gob.mx/cofepris a través de VigiFlow, e-Reporting o al correo farmacovigilancia@cofepris.gob.mx
Por último, precisó que la Coepriss seguirá con las acciones de vigilancia para evitar que las empresas o establecimientos incumplan con la legislación sanitaria vigente y que los productos que sean comercializados en Sinaloa no representen un riesgo a la población. "Se aplicarán medidas de seguridad en establecimientos que los distribuyan o comercialicen, asegurando los medicamentos ilegales, así como imponiendo las sanciones administrativas que resulten procedentes por infringir la regulación sanitaria vigente", advirtió.